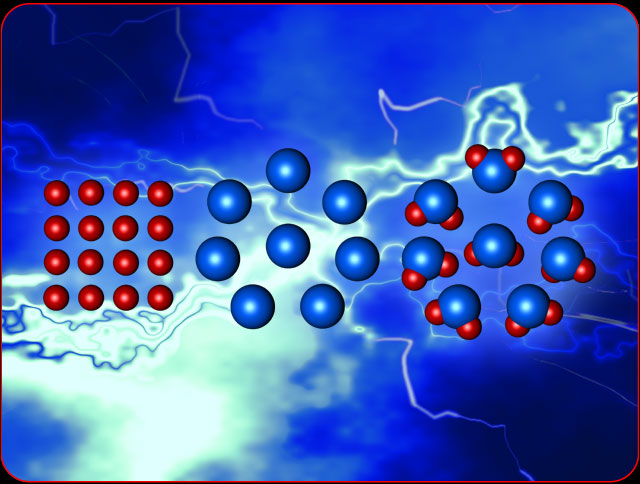
 Moleküllerin ve buna bağlı olarak da maddenin oluşması için atomların aralarındaki çeşitli bağlar oluşturmaları gerekir. Bu işlemler yeryüzündeki madde çeşitliliğinin kilit noktasını oluşturur. Bu konu hakkında bilgi sahibi olan ve düşünen her insan Allah ' ın benzeri olmayan azametine şahit olacak ve Rabbimizin şanını yüceltecektir.
Moleküllerin ve buna bağlı olarak da maddenin oluşması için atomların aralarındaki çeşitli bağlar oluşturmaları gerekir. Bu işlemler yeryüzündeki madde çeşitliliğinin kilit noktasını oluşturur. Bu konu hakkında bilgi sahibi olan ve düşünen her insan Allah ' ın benzeri olmayan azametine şahit olacak ve Rabbimizin şanını yüceltecektir. Birçok madde aynı atomları içermesine rağmen farklı görünür ve farklı özellikler taşır. Bunun da nedeni atomların molekülleri oluşturmak için aralarında kurdukları farklı kimyasal bağlardır.
Maddeye giden ilk basamak olan atomlardan sonra ikinci basamak moleküllerdir. Moleküller, maddenin kimyasal özelliklerini belirten en küçük birimlerdir. Bu küçük yapılar iki veya daha çok atomdan, bazıları da binlerce atom grubundan oluşur. Atomları, molekül içinde elektromanyetik çekim kuvvetine dayalı kimyasal bağlar bir arada tutarlar. Bu bağlar atomların sahip oldukları elektrik yüklerini esas alarak kurulurlar. Atomların elektrik yükleri de daha önce belirttiğimiz gibi son yörüngelerinde taşıdıkları elektronlar tarafından belirlenir. Moleküllerin çeşitli biçimlerde bir araya gelmeleriyle de çevremizde gördüğümüz madde çeşitliliği ortaya çıkar. Bu noktada da maddenin çeşitliliğinin ana merkezinde yer alan kimyasal bağların önemi anlaşılır.
Kimyasal Bağlar
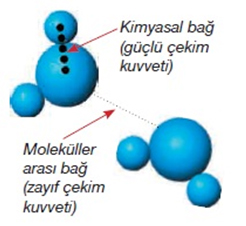
Kimyasal bağlar, atomların dış yörüngelerindeki elektronların hareketleriyle oluşur. Her atom en dışta yer alan yörüngesini, alabileceği en fazla elektron sayısına tamamlama gayreti içindedir. Atomlar son yörüngelerinde bulundurabilecekleri maksimum elektron sayısına ulaşmaya çalışırken ya en dış yörüngelerindeki elektronları maksimuma tamamlamak için başka atomlardan elektron alırlar, ya da eğer en dış yörüngelerinde az sayıda elektron varsa, bunları bir başka atoma vererek önceden tamamlanmış olan bir alt yörüngeyi en dış yörüngeleri haline getirirler. Atomların son yörüngesini maksimuma tamamladıktan sonra oluşan hallerine ise 'kararlılık hali' denir. Atomların kendi aralarındaki bu elektron alıp verme eğilimi, birbirleri arasında yaptıkları kimyasal bağların temel itici gücünü oluşturur.
Bu itici güç, yani atomların son yörüngelerindeki elektron sayılarını maksimuma tamamlama amaçları, bir atomun diğer atomlarla 3 çeşit bağ kurabilmesini sağlar. Bunlar iyonik bağ, kovalent bağ ve metalik bağdır.
Moleküller arasında ise genel olarak "zayıf bağlar" başlığı altında toplanan özel bağlar görev yapar. Bu bağların özellikleri nedir ve nasıl kurulurlar, kısaca ele alalım.
İyonik Bağlar
(4).jpg)
Bu bağ ile birleşen atomlar son yörüngelerindeki elektron sayısını maksimuma, örneğin 8 ' e tamamlamak için birbirleriyle elektron alışverişinde bulunurlar. Son yörüngelerinde 4 ' e kadar elektronu bulunan atomlar bu elektronları birleşecekleri yani bağ kuracakları atoma verirler. Son yörüngelerinde 4 ' ten fazla elektron bulunduran atomlar ise birleşecekleri yani bağ kuracakları atomlardan elektron alırlar. Bu tip bağ ile oluşan moleküller kübik yapıya sahip olurlar. Yakından tanıdığımız sofra tuzu molekülleri bu bağ ile oluşmuş maddelerden biridir. Peki, atomların neden böyle bir eğilimi vardır? Bu eğilim olmasa ne olurdu?
Bugüne kadar atomların bir araya gelmek için aralarında kurdukları bağlar çok genel biçimde tarif edilebilmiştir. Ama atomların neden böyle bir prensiple davrandıkları anlaşılamamıştır. Yoksa atomlar son yörüngelerindeki elektronların sayısının 8 olması gerektiğini kendileri mi tespit etmiştir? Tabii ki hayır. Bu öyle bir sayıdır ki, maddenin ve dolayısıyla evrenin meydana gelmesi için ilk basamak olan atomların birleşmelerindeki kilit noktadır. Eğer atomların bu prensipten kaynaklanan eğilimleri olmasaydı moleküller ve buna bağlı olarak da madde oluşamazdı.
Oysa atomlar ilk yaratıldıkları andan itibaren sahip oldukları bu eğilim sayesinde moleküllerin ve maddenin kusursuz bir biçimde meydana gelmesi için hizmet ederler.
Kovalent Bağlar
(2).jpg) Atomların arasındaki bağları inceleyen bilim adamları ilginç bir durumla karşılaştılar. Bazı atomlar bağ kurmak için elektron alışverişinde bulunurken, bazıları da son yörüngelerindeki elektronları ortak kullanmaktaydılar. Daha sonra yapılan çalışmalarda canlılık için vazgeçilmez önem taşıyan birçok molekülün bu bağlar sayesinde var olabildiğini ortaya koymuştur.
Atomların arasındaki bağları inceleyen bilim adamları ilginç bir durumla karşılaştılar. Bazı atomlar bağ kurmak için elektron alışverişinde bulunurken, bazıları da son yörüngelerindeki elektronları ortak kullanmaktaydılar. Daha sonra yapılan çalışmalarda canlılık için vazgeçilmez önem taşıyan birçok molekülün bu bağlar sayesinde var olabildiğini ortaya koymuştur. Kovalent bağın daha iyi anlaşılabilmesi için kolay bir örnek verelim: Daha önce elektron yörüngelerinden bahsederken de belirttiğimiz gibi atomların ilk yörüngelerinde en fazla 2 elektron taşınabilir. Hidrojen atomu tek bir elektrona sahiptir ve elektron sayısını 2 ' ye çıkarıp kararlı bir atom olma eğilimindedir. Bu yüzden hidrojen atomu ikinci bir hidrojen atomuyla kovalent bağ yapar. Yani, 2 hidrojen atomu da birbirlerinin tek elektronlarını 2. elektron olarak kullanır. Böylece H2 molekülü oluşur.
Metalik Bağlar
.jpg) Eğer çok sayıda atom, birbirlerinin elektronlarını ortaklaşa kullanarak birleşiyorlarsa, bu kez "metalik bağ" söz konusudur. Günlük hayatta çevremizde gördüğümüz ya da kullandığımız pek çok araç ve gerecin ana maddesini oluşturan demir, bakır, çinko, alüminyum gibi metaller, kendilerini oluşturan atomların birbirleri aralarında metalik bağlar yapmaları sonucunda, elle tutulur, gözle görülür, kullanılabilir bir yapı kazanmışlardır.
Eğer çok sayıda atom, birbirlerinin elektronlarını ortaklaşa kullanarak birleşiyorlarsa, bu kez "metalik bağ" söz konusudur. Günlük hayatta çevremizde gördüğümüz ya da kullandığımız pek çok araç ve gerecin ana maddesini oluşturan demir, bakır, çinko, alüminyum gibi metaller, kendilerini oluşturan atomların birbirleri aralarında metalik bağlar yapmaları sonucunda, elle tutulur, gözle görülür, kullanılabilir bir yapı kazanmışlardır. Atomların yörüngelerindeki elektronların neden böyle bir eğilimi olduğu sorusunu ise bilim adamları cevaplayamamaktadır. Fakat canlı organizmalar ancak nedenini bilmediğimiz bu eğilim sayesinde var olabilirler.
Acaba tüm bu bağlarla kaç farklı bileşik oluşabilmektedir?
Laboratuarlarda her gün yeni bileşikler oluşturulmaktadır. Şu an için yaklaşık 2 milyon bileşikten bahsetmek mümkündür. En basit kimyasal bileşik, hidrojen molekülü kadar ufak olabildiği gibi, milyonlarca atomdan oluşan bileşikler de vardır.
Bir element acaba en fazla kaç değişik bileşik oluşturabilir? Bu sorunun cevabı oldukça ilginçtir. Çünkü bir tarafta hiçbir elementle birleşmeyen bazı elementler (soy gazlar) vardır. Diğer tarafta ise 1.700.000 bileşik oluşturabilen karbon atomu vardır. Toplam bileşik sayısının 2 milyon kadar olduğunu tekrar hatırlarsak, 109 elementin 108 ' i toplam 300.000 bileşik yapmaktadırlar. Ancak karbon olağanüstü bir şekilde tek başına tam 1.700.000 bileşik yapabilmektedir.
Karbon atomunun bu olağanüstü özelliği yeryüzünün hiçbir şekilde taklit edilemeyecek sistemlerle donatılmış olduğunun delillerindendir. Yüce Rabbimiz yeryüzünü insanın emrine bir nimet olarak sunmuştur. Bize düşen de bu nimetin şükrünü yerine getirmektir.
Bu makale, Mercek Dergisi 16. sayı (Ekim 2002) 24. sayfada yayınlanmıştır.


