Chapitre 3: La seconde étape vers la matière: les molécules
La Seconde Étape Vers La Matière: Les Molécules
Qu'est-ce qui rend tous les objets que vous apercevez autour de vous différents les uns des autres? Qu'est-ce qui différencie leurs couleurs, leurs formes, leurs odeurs et leurs goûts? Pourquoi une substance est-elle molle, une autre dure, et une autre liquide? De ce que vous avez lu jusqu'à maintenant, vous pouvez répondre à ces questions en disant: "C'est à cause des différences entre leurs atomes." Cependant, cette réponse n'est pas suffisante, car si les atomes étaient la cause de leurs différences, alors il devrait y avoir des milliards d'atomes portant différentes propriétés les unes des autres. En pratique, ce n'est pas le cas. Beaucoup de matériaux ont l'air différent et ont des propriétés différentes bien qu'ils contiennent les mêmes atomes. La raison à cela est la différence des liaisons chimiques que les atomes forment entre eux pour devenir des molécules.
Sur le chemin qui mène à la matière, les molécules sont la seconde étape après les atomes. Les molécules sont les plus petites unités déterminant les propriétés chimiques de la matière. Ces petits corps sont constitués de deux ou de plusieurs atomes et certains, de centaines de groupes d'atomes. Les atomes sont assemblés dans les molécules par des liaisons chimiques déterminées par la force électromagnétique d'attraction, ce qui signifie que ces liaisons sont formées sur la base des charges électriques des atomes. Les charges électriques des atomes, à leur tour, sont déterminées par les électrons de leur couche externe. L'arrangement des molécules selon différentes combinaisons donne naissance à la diversité de la matière que nous voyons autour de nous. L'importance des liaisons chimiques qui constituent le cœur de la diversité de la matière apparaît donc à ce niveau.
Les liaisons chimiques
Comme on l'a expliqué ci-dessus, les liaisons chimiques sont formées à travers le mouvement des électrons de la couche externe des atomes. Chaque atome a tendance à remplir sa couche externe avec le nombre maximal d'électrons qu'il peut abriter. Le nombre maximal d'électrons que les atomes peuvent supporter dans leur couche externe est 8. Pour faire cela, soit les atomes reçoivent des électrons d'autres atomes pour compléter leur nombre d'électrons dans leur couche externe à huit, ou, s'ils ont moins d'électrons dans leur couche externe, ils les donnent alors à un autre atome, en créant une sous-couche qui était auparavant complète. La tendance des atomes à échanger des électrons constitue la force incitant les liaisons chimiques à se former entre eux.
Cette force motrice, c'est-à-dire l'objectif des atomes à augmenter le nombre des électrons de leur couche externe au maximum, force un atome à former trois types de liaisons avec d'autres atomes. Ce sont la liaison ionique, la liaison covalente et la liaison métallique.
Couramment, des liaisons spéciales catégorisées sous le titre général de "liaisons faibles" agissent entre les molécules. Ces liaisons sont plus faibles que les liaisons formées par les atomes qui constituent ces molécules car les molécules ont besoin de structures plus flexibles pour former la matière.
Examinons maintenant, rapidement, les propriétés de ces liaisons et la manière dont elles se forment.
Les liaisons ioniques
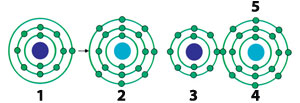
1) Atome de sodium
2) Atome de chlore
3) Ion de sodium
4) Ion de chlore
5) Molécule de chlore de sodium (NaCl)
L'atome de sodium donne son électron de la couche supérieure à un atome de chlore et devient ainsi chargé positivement. En recevant l'électron, l'atome de chlore devient chargé négativement. Les deux forment une liaison ionique à travers ces deux charges opposées qui s'attirent l'une l'autre.24
Les atomes combinés par cette liaison échangent des électrons afin de compléter le nombre d'électrons de leur couche externe à huit. Les atomes ayant jusqu'à quatre électrons dans leur couche externe donnent ces électrons à l'atome avec lequel ils vont se combiner, c'est-à-dire avec lequel ils vont se lier. Les atomes qui ont plus de quatre électrons dans leur couche externe reçoivent des électrons des atomes avec lesquels ils vont se lier. Les molécules formées par ce type de liaison ont des structures cristallines (cubiques). Les molécules du sel de table commun (NaCl) font partie des substances formées par cette liaison. Pourquoi les atomes ont-ils cette tendance? Qu'arriverait-il s'ils ne l'avaient pas?
Est-ce que les atomes peuvent décider par eux-mêmes que le nombre d'électrons dans leur couche externe doit être de huit? Absolument pas. C'est un comportement tellement décisif qu'il dépasse l'atome, car celui-ci n'a pas d'intellect, de volonté ou de conscience. Ce nombre est la clé dans la combinaison des atomes en molécules qui constitue la première étape de la création de la matière et, au final, de l'univers. Si les atomes n'avaient pas un tel comportement basé sur ce principe, certaines des molécules nécessaires à la vie n'existeraient pas. Cependant, à partir de l'instant où ils furent créés, les atomes ont servi à la formation des molécules et de la matière selon un ordre parfait grâce à ce comportement.
Les liaisons covalentes
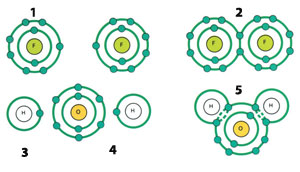
1) Atome de fluor 2) Molécule de fluor (F2)
3) Atome d'hydrogène 4) Atome d'oxygène
5) Molécule d'eau (H2O)
Certains atomes forment de nouvelles molécules grâce aux liaisons covalentes,en partageant leurs électrons respectifs situés dans leurs orbites externes.25
Les scientifiques qui ont étudié les liaisons entre atomes ont fait face à une situation intéressante. Tandis que certains atomes échangent des électrons pour se lier, d'autres partagent les électrons de leur couche externe. Des recherches plus avancées ont révélé qu'un grand nombre de molécules qui sont d'une importance critique pour la vie doivent leur existence à ces liaisons "covalentes".
Prenons un exemple simple pour mieux expliquer les liaisons covalentes. Comme on l'a mentionné précédemment au sujet des couches électroniques, les atomes peuvent transporter un maximum de deux électrons dans leur couche la plus interne. L'atome d'hydrogène possède un seul électron et a tendance à augmenter le nombre de ses électrons à deux pour devenir un atome stable. Par conséquent, l'atome d'hydrogène forme une liaison covalente avec un second atome d'hydrogène. C'est-à-dire que les deux atomes d'hydrogène partagent l'électron de l'autre en tant que second électron. Ainsi, une molécule de H2 se forme.
Les liaisons métalliques
Si un grand nombre d'atomes s'assemblent en partageant les électrons des autres, cela s'appelle une "liaison métallique". Les métaux comme le fer, le cuivre, le zinc, l'aluminium etc. qui forment la matière première de nombreux outils et instruments que nous voyons et utilisons tous les jours, ont acquis un corps substantiel et tangible suite aux liaisons métalliques formées par les atomes qui les constituent.
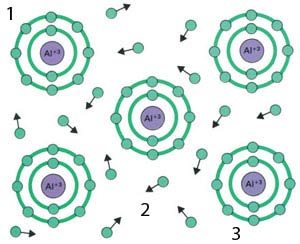
1) Liaison métallique
2) Electron
3) Ion d'aluminium
Les liaisons entre les atomes de métal sont très différentes des autres formes de liaisons chimiques – chaque atome de métal met son électron externe en commun. Cette "mer d'électrons" explique une propriété clé des métaux – leur capacité à conduire l'électricité.26
L'étape suivante: les composés
Imaginez-vous combien de composés différents ces liaisons peuvent former?
En laboratoire, de nouveaux composés sont produits tous les jours. À l'heure actuelle, il est possible de parler de pratiquement deux millions de composés. Le plus simple composé chimique peut être aussi petit que la molécule d'hydrogène, tandis qu'il existe également des composés constitués de millions d'atomes.27
Combien de composés différents un élément peut-il former au maximum? La réponse à cette question est vraiment intéressante car, d'un côté, il existe des éléments qui n'interagissent avec aucun autre (les gaz inertes) tandis que, d'un autre côté, il y a l'atome de carbone qui est capable de former 1.700.000 composés. Comme énoncé ci-dessus, le nombre total de composés est d'environ deux millions. 108 éléments sur les 109 forment 300.000 composés. Le carbone, cependant, forme 1.700.000 composés, de lui-même, d'une manière plutôt stupéfiante.
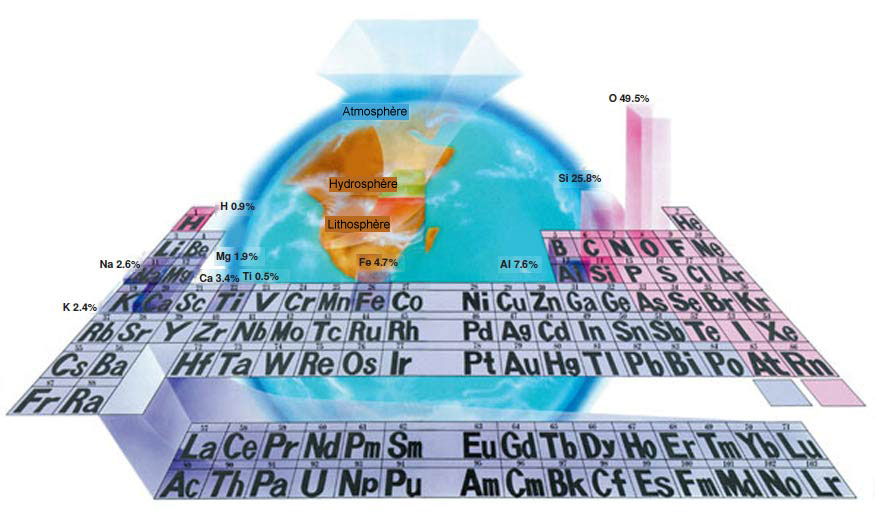
Les matières premières de l'univers et le tableau périodique: 92 éléments libres dans la nature et 17 éléments fabriqués artificiellement dans des laboratoires ou dans des réacteurs nucléaires sont organisés dans un tableau appelé "tableau périodique" en fonction du nombre de leurs protons. À première vue, le tableau périodique peut paraître être un groupe de boîtes contenant une ou deux lettres ainsi que des nombres situés sur le haut et le bas des côtés. Ce qui est plus intéressant est que ce tableau contient les éléments de l'univers entier y compris les constituants de l'air que nous respirons et les éléments de notre corps.
La brique de la vie: l'atome de "carbone"
L'atome de carbone
Le carbone est l'élément le plus vital pour les êtres vivants, car tous les organismes vivants sont construits à partir de composés de carbone. De nombreuses pages ne seraient pas suffisantes pour décrire les propriétés de l'atome de carbone, qui est extrêmement important pour notre existence. Nous n'allons mentionner ici que quelques-unes des propriétés très importantes du carbone.
Des structures aussi diverses que la membrane d'une cellule, les bois d'un élan, le tronc d'un séquoia, le cristallin de l'œil, et le venin d'une araignée sont composées à partir de carbone. Le carbone, combiné avec de l'hydrogène, de l'oxygène et de l'azote selon différentes quantités et arrangements géométriques, aboutit à un vaste assortiment de matériaux ayant des propriétés extrêmement différentes. Quelle est donc la raison de la capacité du carbone à former approximativement 1,7 million de composés?
Une des propriétés les plus importantes du carbone est sa capacité à former très facilement des chaînes en alignant des atomes les uns après les autres. La chaîne la plus courte est constituée de deux atomes de carbone. En dépit de l'indisponibilité d'un chiffre exact du nombre d'atomes de carbone qui constituent la plus grande chaîne, on peut parler d'une chaîne d'environ soixante-dix liens. Si l'on considère que l'atome qui peut former la plus grande chaîne après l'atome de carbone est l'atome de silicium qui peut former six liens, on comprend mieux la position exceptionnelle de l'atome de carbone.28
La raison de la capacité du carbone à former des chaînes avec autant de liens tient au fait que ses chaînes ne sont pas forcément linéaires. Elles peuvent se ramifier, comme elles peuvent former des polygones.
TROIS MOLÉCULES SIMILAIRES
RÉSULTAT: TROIS SUBSTANCES TRÈS DIFFÉRENTES
Même une différence de quelques atomes entre les molécules conduit à des résultats très différents. Par exemple, regardez attentivement les deux molécules ci-dessous. Elles paraissent très similaires exception faite d'une petite différence au niveau de leurs atomes de carbone et d'hydrogène. Le résultat est deux substances complètement opposées:
C18H24O2 and C19H28O2
Pourriez-vous deviner ce que ces molécules représentent? La première est l'oestrogène, l'autre est la testostérone. C'est-à-dire que la première est l'hormone responsable des caractéristiques femelles et la deuxième est responsable des caractéristiques mâles. Ce qui est donc intéressant à constater est que même une différence de quelques atomes peut provoquer des différences sexuelles.
À présent, regardez la formule ci-dessous:
C6H12O2
N'est-il pas vrai que cette molécule ressemble aux molécules des hormones de testostérone et d'oestrogène? Quelle est donc cette molécule, est-ce une autre hormone? Répondons tout de suite: c'est la molécule du sucre.
À partir de l'exemple de ces trois molécules composées d'éléments du même type, il devient clair que la différence dans le nombre d'atomes peut produire des substances diverses. D'une part, il y a les hormones responsables des caractéristiques sexuelles, et d'autre part il y a le sucre, un élément de base de l'alimentation.
À ce niveau, la formation de la chaîne joue un rôle très important. Dans deux composés carbonés, par exemple, si les atomes de carbone sont en même nombre mais combinés selon différentes formes de chaînes, deux substances différentes sont formées. Les caractéristiques de l'atome de carbone mentionnées ci-dessus produisent des molécules qui sont critiques pour la vie.
Certaines molécules de composés carbonés ne sont constituées que de quelques atomes; d'autres en contiennent des milliers ou même des millions. Aucun autre élément n'a autant d'usages que le carbone dans la formation de molécules avec une telle stabilité et solidité. En citant David Burnie dans son livre Life (La vie):
Le carbone est un élément vraiment extraordinaire. Sans la présence du carbone et de ses propriétés rares, il n'y aurait probablement pas de vie sur Terre.29
Concernant l'importance du carbone pour les êtres vivants, le chimiste britannique Nevil Sidgwick écrit dans Chemical Elements and Their Compounds (Les Éléments Chimiques et Leurs Composés):
Le carbone est unique parmi les éléments de par le nombre et la variété des composés qu'il peut former. Plus d'un quart de million ont déjà été isolés et décrits, mais cela ne donne qu'une idée très imparfaite de sa puissance, puisqu'il est la base de toutes les formes de matière vivante.30

Le diamant, qui est une pierre très précieuse, est un dérivé du carbone qui se trouve dans la nature à l'état de graphite.
Le groupe des composés formés exclusivement de carbone et d'hydrogène sont appelés "composés hydrocarbonés". C'est une famille immense de composés qui comprend le gaz naturel, le pétrole liquide, le kérosène et les huiles lubrifiantes. L'éthylène et le propylène forment la base de l'industrie pétrochimique. Les composés hydrocarbonés du type benzène, toluène et térébenthine sont familiers des gens qui ont travaillé avec des peintures. Le naphtalène qui protège nos vêtements des mites est un autre composé hydrocarboné. Les composés hydrocarbonés combinés avec du chlore ou du fluor forment les anesthésiques, les produits chimiques utilisés dans les extincteurs et les Fréons utilisés dans la réfrigération.
Comme le citait le chimiste Sidgwick, l'esprit humain est incapable de comprendre pleinement le potentiel de cet atome qui n'a que six protons, six neutrons et six électrons. Il est impossible que la moindre propriété de cet atome, qui est vital pour la vie, se soit formée par hasard. En bref, Dieu, qui embrasse toute chose jusqu'aux atomes, a créé l'atome de carbone sous une forme parfaitement compatible avec les corps des êtres vivants.
C'est à Dieu qu'appartient tout ce qui est dans les cieux et sur la terre. Et Dieu embrasse toute chose. (Sourate an-Nisa: 126)
Les liaisons intermoléculaires: les liaisons faibles
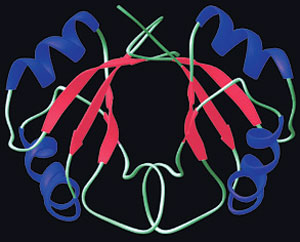
La séquence des acides aminés et la configuration tridimensionnelle déterminent la fonction de la protéine à l'intérieur du corps. Les liaisons faibles entre ces molécules forment ces structures.
Les liaisons combinant les atomes sont plus fortes que les liaisons intermoléculaires faibles. Ces liaisons peuvent aider à la formation de millions, voire de milliards de types de molécules.
Alors, comment les molécules se combinent-elles pour former la matière?
Puisque les molécules deviennent stables après leur formation, elles n'échangent plus d'atomes.
Donc, qu'est-ce qui les maintient ensemble?
Afin de répondre à cette question, les chimistes ont produit différentes théories. Leurs recherches ont montré que les molécules sont capables de se combiner selon différentes manières en fonction des propriétés de leurs atomes.
Ces liaisons sont très importantes pour la chimie organique, qui est la chimie des êtres vivants, car les molécules les plus importantes qui constituent la vie se forment grâce à leur capacité à former ces liaisons. Prenons l'exemple des protéines. Les formes complexes tridimensionnelles des protéines, qui sont les briques des êtres vivants, se forment grâce à ces liaisons. Cela signifie que la liaison chimique faible existant entre ces molécules est au moins autant nécessaire que la liaison chimique forte existant entre les atomes pour former la vie. Il est certain que la force de ces liaisons doit avoir une valeur précise.
Que se passerait-il si les atomes proches d'autres
atomes réagissaient immédiatement?
 |
|---|
Nous venons de dire que l'univers entier est formé de l'interaction des atomes de 109 éléments différents. Il y a un point qui a besoin d'être mentionné, qui est qu'une condition très importante doit être remplie pour que la réaction commence.
Par exemple, l'eau ne se forme jamais quand de l'oxygène et de l'hydrogène se rapprochent et le fer ne rouille pas dès qu'il entre en contact avec de l'air. S'il le faisait, le fer, qui est un métal dur et brillant, se transformerait en oxyde ferreux, qui est une poudre, en quelques minutes et l'ordre du monde serait grandement perturbé. Si les atomes qui se rapprochaient entre eux à une certaine distance s'unissaient immédiatement sans remplir certaines conditions, les atomes de deux substances différentes interagiraient aussitôt. Dans ce cas, il vous serait impossible de vous asseoir sur une chaise, car les atomes formant la chaise réagiraient immédiatement avec les atomes formant votre corps et vous deviendriez une chose à mi-chemin entre une chaise et un humain (!). Bien sûr, dans un tel monde, la vie serait impossible. Comment cela est-il évité?
Pour donner un exemple, les molécules d'hydrogène et d'oxygène réagissent très lentement à température ambiante. Cela signifie que l'eau se forme très lentement à température ambiante. Cependant, quand la température de l'environnement augmente, l'énergie des molécules augmente également et les réactions sont accélérées, et ainsi l'eau se forme plus rapidement.
La quantité minimale d'énergie nécessaire pour que les molécules réagissent entre elles est appelée "l'énergie d'activation". Par exemple, afin que les molécules d'hydrogène et d'oxygène réagissent entre elles pour former de l'eau, leur énergie doit être supérieure à l'énergie d'activation.
Réfléchissons. Si la température sur Terre était un peu plus élevée, les atomes réagiraient trop vite, ce qui détruirait l'équilibre de la nature. Si l'opposé était vrai, c'està- dire si la température sur Terre était moins élevée, alors les atomes réagiraient trop lentement, ce qui perturberait à nouveau l'équilibre de la nature. Comme on le voit, la distance entre la Terre et le Soleil est tout juste appropriée au support de la vie sur Terre. Les équilibres délicats nécessaires à la vie ne s'arrêtent pas là. L'inclinaison de l'axe de la Terre, sa masse, sa surface, la proportion des gaz de son atmosphère, la distance entre la Terre et son satellite, la Lune, et bien d'autres facteurs doivent avoir leurs valeurs actuelles pour que les êtres vivants puissent survivre. Cela amène au fait que tous ces facteurs n'ont pas pu se former progressivement par hasard, et qu'ils ont tous été créés par Dieu, Celui qui possède la puissance suprême, qui connaît toutes les propriétés des êtres vivants.
Traditionnellement, le rôle de la science au cours de ces processus n'est que de nommer les lois de physique qu'elle observe. Comme on l'a expliqué au début, dans le cas de tels phénomènes, des questions du type "quoi?", "comment?" et "de quelle manière?" deviennent insignifiantes. Ce que nous pouvons atteindre avec ces questions n'est que le détail d'une loi existante. Les questions principales qui doivent être posées sont "pourquoi?" et "qui a créé cette loi?". La réponse à ces questions reste une énigme pour les scientifiques qui adhèrent aveuglément à leurs dogmes matérialistes.
À ce stade, où les matérialistes sont dans une impasse, le dessin est très clair pour une personne qui observe les événements en utilisant son esprit et sa conscience. Les équilibres parfaits de l'univers, qui ne peuvent être expliqués par des coïncidences, sont apparus grâce au commandement d'un esprit et d'une volonté suprême, comme l'énonce ce verset: "…Certes, Dieu tient compte de tout". (Sourate an-Nisa: 86), et Il a créé toute chose selon un calcul, un ordre et un équilibre très précis.
On peut continuer avec l'exemple des protéines. Les molécules appelées acides aminés se combinent pour former des protéines, qui sont de plus grandes molécules. Les atomes formant les acides aminés se combinent par des liaisons covalentes. Des liaisons faibles combinent ces acides aminés de telle manière à produire des motifs tridimensionnels. Les protéines ne peuvent fonctionner chez les organismes vivants que si elles possèdent ces motifs tridimensionnels. Par conséquent, si ces liaisons n'existaient pas, ni les protéines, et donc ni la vie, n'existeraient.
La liaison "hydrogène", un type de liaison faible, joue un rôle majeur dans la formation des matériaux qui ont une grande importance dans notre vie. Par exemple, les molécules formant l'eau, qui est la base de la vie, sont réunies par des liaisons hydrogènes.
Une molécule miraculeuse: l'eau
Un liquide spécifiquement choisi pour la vie – "l'eau" – recouvre les deux tiers de notre Terre. Les corps de tous les êtres vivants sur la Terre sont formés à partir de ce liquide très spécial selon une proportion allant de 50 à 95%. Depuis les bactéries vivant dans des sources d'eau chaude à des températures proches du point d'ébullition de l'eau, jusqu'à certaines mousses vivant sur des glaciers, la vie est présente partout où il y a de l'eau, quelle que soit sa température. Même dans une simple goutte restée sur une feuille après la pluie, des milliers d'organismes vivants microscopiques apparaissent, se reproduisent et meurent.
À quoi ressemblerait la Terre s'il n'y avait pas d'eau? Il est certain que tout serait désert. Il y aurait des fosses et des gouffres horribles, à la place des mers. Le ciel n'aurait pas de nuages et aurait une couleur étrange.
En fait, il est extrêmement difficile à l'eau, la base de la vie sur Terre, de se former. Tout d'abord, imaginons que des molécules d'hydrogène et d'oxygène, qui sont les composants de l'eau, soient placées dans un bol en verre. Laissons-les dans le bol pendant un temps très long. Il est fort probable que ces gaz ne formeront toujours pas d'eau même s'ils restent dans le bol pendant des centaines d'années. Même s'ils en forment, ce ne serait pas plus qu'une toute petite quantité dans le fond du bol et cela surviendrait très lentement, peut-être après des milliers d'années.

N'as-tu pas vu que Dieu fait descendre l'eau du ciel, et la terre devient alors verte? Dieu est plein de bonté et parfaitement connaisseur.(Sourate al-Hajj: 63)
La raison pour laquelle l'eau se forme si lentement sous ces circonstances est la température. À température ambiante, l'oxygène et l'hydrogène réagissent très lentement.
L'oxygène et l'hydrogène, lorsqu'ils sont libres, se trouvent sous la forme de molécules de H2 et d'O2. Pour s'unir pour former une molécule d'eau, ils doivent rentrer en collision. Suite à cette collision, les liaisons formant les molécules d'hydrogène et d'oxygène se fragilisent, ce qui permet l'union des atomes d'oxygène et d'hydrogène. La température augmente l'énergie et donc la vitesse de ces molécules, ce qui aboutit à une augmentation du nombre de collisions. Ainsi, elle accélère la vitesse de la réaction. Cependant, actuellement, aucune température assez élevée pour former de l'eau n'existe sur Terre. La chaleur requise pour la formation de l'eau a été fournie au cours de la formation de la Terre, ce qui a abouti à l'apparition d'assez d'eau pour recouvrir les trois quarts de la surface terrestre. Maintenant, l'eau s'évapore et grimpe dans l'atmosphère où elle refroidit et retourne sur terre sous forme de pluie. C'est-à-dire qu'il n'y pas d'augmentation de sa quantité, mais seulement un cycle perpétuel.
Les propriétés miraculeuses de l'eau
L'eau a de nombreuses propriétés chimiques exceptionnelles. Chaque molécule d'eau se forme par l'union d'atomes d'hydrogène et d'oxygène. Il est intéressant de noter que ces deux gaz, l'un comburant et l'autre combustible, s'unissent pour former un liquide, et qui plus est, l'eau.
Maintenant, étudions brièvement comment l'eau est formée chimiquement. La charge électrique de l'eau est de zéro, c'est-à-dire qu'elle est neutre. Cependant, à cause des tailles des atomes d'oxygène et d'hydrogène, l'oxygène de la molécule d'eau possède une légère charge négative et l'hydrogène une légère charge positive. Quand plusieurs molécules d'eau se rapprochent, les charges positives et négatives s'attirent entre elles pour former une liaison spéciale appelée "liaison hydrogène". La liaison hydrogène est une liaison très faible et a une durée de vie extrêmement courte. La durée d'une liaison hydrogène est d'environ un centième de milliardième de seconde. Mais dès qu'une liaison se casse, une autre se forme. Ainsi, les molécules d'eau adhèrent fortement aux autres tout en conservant leur forme liquide car elles sont réunies par des liaisons faibles.
Les liaisons hydrogènes permettent aussi à l'eau de résister aux changements de température. Même si la température de l'air augmente soudainement, la température de l'eau augmente doucement, et de la même manière, si la température de l'air chute brusquement, la température de l'eau diminue doucement. De grands changements de température sont nécessaires pour provoquer des changements considérables dans la température de l'eau. L'énergie thermique très importante de l'eau apporte des bénéfices majeurs à la vie. Pour donner un exemple simple, il y a une grande quantité d'eau dans nos corps. Si l'eau s'adaptait aux changements soudains de la température de l'air à la même vitesse, nous serions brusquement fiévreux ou glacés.
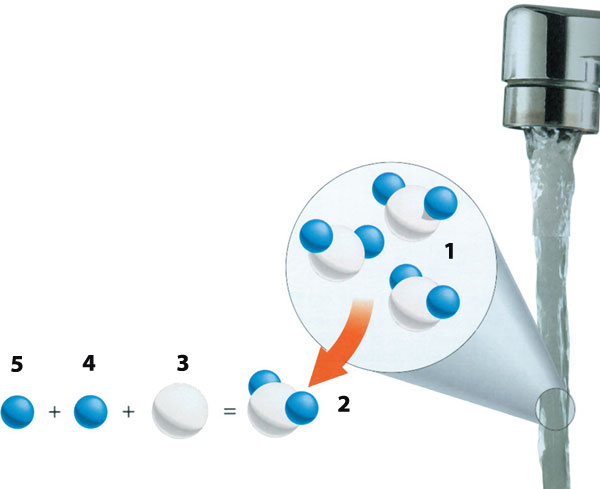
1) Molécule d'eau 2) H2O 3) Oxygène 4) Hydrogène 5) Hydrogène
De la même façon, l'eau a besoin d'une énergie thermique considérable pour s'évaporer. Puisque l'eau utilise une grande quantité d'énergie thermique quand elle s'évapore, sa température diminue. Pour donner un exemple, une nouvelle fois lié au corps humain, la température normale du corps est de 36°C et la température la plus élevée que nous pouvons tolérer est de 42°C. Cet intervalle de 6°C est en fait très petit et le simple fait de travailler sous le soleil pendant quelques heures peut augmenter la température du corps de cette quantité. Cependant, nos corps dépensent une grande quantité d'énergie thermique à travers la transpiration, c'est-à-dire en forçant l'eau qu'ils contiennent à s'évaporer, ce qui à son tour provoque la diminution de la température corporelle. Si nos corps ne possédaient pas un tel mécanisme automatique, travailler quelques heures sous le soleil serait fatal.

Si l'eau ne possédait pas la propriété de geler à partir de la surface vers le bas, une quantité importante des mers serait gelée au cours d'une année et la vie dans la mer serait mise en danger.
Les liaisons hydrogènes dotent l'eau d'une autre propriété extraordinaire, qui fait que l'eau est plus dense dans son état liquide que dans son état solide. En règle générale, la plupart des substances sur terre sont plus denses dans leur état solide que dans leur état liquide. Contrairement à ces substances, cependant, l'eau se dilate quand elle gèle. Car les liaisons hydrogènes empêchent les molécules d'eau de se lier aux autres trop fortement, et ainsi de nombreux espaces se forment entre elles. Les liaisons hydrogènes se cassent quand l'eau est sous son état liquide, ce qui force les atomes d'oxygène à se rapprocher les uns des autres et ce qui forme une structure plus dense.
Cela amène également la glace à être plus légère que l'eau. Normalement, si vous fondez du métal et lancez dedans quelques pièces solides du même métal, ces pièces vont couler directement au fond. Dans l'eau, cependant, les choses sont différentes. Des icebergs pesant des dizaines de milliers de tonnes flottent sur l'eau comme des bouchons. Quel bénéfice peut-on retirer de cette propriété de l'eau?

À cause du fait que la densité de l'eau gelée est inférieure à celle de l'eau à l'état liquide, les blocs de glace flottent sur l'eau.
Répondons à cette question avec l'exemple d'une rivière: quand le temps est froid, ce n'est pas toute la rivière mais seulement sa surface qui gèle. L'eau atteint son état le plus lourd à +4°C, et dès qu'elle atteint cette température, elle coule immédiatement au fond. La glace se forme sur le dessus de l'eau comme une couche. Sous cette couche, l'eau continue de circuler, et puisque +4°C est une température à laquelle les organismes vivants peuvent survivre, la vie dans l'eau continue.
Ces propriétés uniques dont Dieu a doté l'eau rendent la vie possible sur la Terre. Dans le Coran, Dieu énonce l'importance de cette bénédiction qu'Il offre à l'homme:
C'est Lui qui, du ciel, a fait descendre de l'eau qui vous sert de boisson et grâce à laquelle poussent des plantes dont vous nourrissez vos troupeaux. D'elle, Il fait pousser pour vous, les cultures, les oliviers, les palmiers, les vignes et aussi toutes sortes de fruits. Voilà bien là une preuve pour des gens qui réfléchissent. (Sourate an-Nahl: 10-11)
Une propriété intéressante de l'eau
Nous savons tous que l'eau bout à 100°C et gèle à 0°C. En fait, sous des circonstances ordinaires l'eau ne devrait pas bouillir à 100°C mais à 180°C. Pourquoi?
Dans la table périodique, les propriétés des éléments du même groupe varient progressivement des éléments légers vers les éléments lourds. Cet ordre est plus évident dans les composés de l'hydrogène. Les composés des éléments partageant le même groupe que l'oxygène dans la table périodique sont appelés "hybrides". En fait, l'eau est un "hybride d'oxygène". Les hybrides d'autres éléments dans ce groupe ont la même structure moléculaire que la molécule d'eau.

Les molécules à la surface d'un liquide subissent une force d'attraction vers l'intérieur. Ceci est la tension de surface. Elle fournit une force de cohésion aux molécules situées à la surface, ce qui est suffisant pour empêcher les pieds d'une araignée d'eau de crever la surface.31
Les points d'ébullition de ces composés varient progressivement du soufre vers les plus lourds; cependant, le point d'ébullition de l'eau va, de manière inattendue, à l'encontre de cet ordre. L'eau (hybride d'oxygène) bout à 80°C en dessous de la température supposée. Un autre fait surprenant concerne le point de congélation de l'eau. Une nouvelle fois, selon l'ordre dans le système périodique, l'eau est supposée geler à -100°C. Mais l'eau casse cette règle et gèle à 0°C, 100°C au-dessus de la température attendue. Cela amène à se poser la question: pourquoi aucun autre hybride, mais seulement l'eau, désobéit aux règles du système périodique?
Les lois de la physique, les lois de la chimie, et toutes les autres choses que nous nommons des règles, ne sont que des tentatives d'explication de l'équilibre extraordinaire de l'univers et des détails de la création. Toutes les recherches menées au 20ème siècle montrent, comme jamais auparavant, que tous les équilibres physiques de l'univers sont taillés sur mesure pour la vie humaine. Les recherches révèlent que toutes les lois de la physique, de la chimie et de la biologie régnant dans l'univers, tout autant que l'atmosphère, le Soleil, les atomes et les molécules etc. sont tous arrangés comme il faut afin de supporter la vie humaine. L'eau, comme les autres éléments mentionnés ci-dessus, est adaptée à la vie avec une telle précision qu'on ne peut la comparer à aucun autre liquide, et une grande partie de la Terre est remplie avec de l'eau en quantité requise pour la vie. Il est évident que tout ceci ne peut être le résultat de coïncidences et qu'il y a un ordre et une conception parfaite prédominant dans l'univers.
Dieu, c'est Lui qui a créé les cieux et la terre et qui, du ciel, a fait descendre l'eau; grâce à laquelle Il a produit des fruits pour vous nourrir. Il a soumis à votre service les vaisseaux qui, par Son ordre, voguent sur la mer. Et Il a soumis à votre service les rivières. Et pour vous, Il a assujetti le Soleil et la Lune à une perpétuelle révolution. Et Il vous a assujetti la nuit et le jour. Il vous a accordé de tout ce que vous Lui avez demandé. Et si vous comptiez les bienfaits de Dieu, vous ne sauriez les dénombrer. L'homme est vraiment très injuste, très ingrat.(Sourate Ibrahim: 32-34)
Les propriétés physiques et chimiques renversantes de l'eau révèlent que ce liquide a été créé spécialement pour la vie humaine. Dieu a donné la vie aux hommes à travers l'eau et grâce à elle a donné naissance depuis la terre à toutes les choses nécessaires à la vie. Dieu appelle les gens à réfléchir à cela dans le Coran:
Et c'est Lui qui, du ciel, a fait descendre l'eau. Puis, par elle Nous fîmes germer toute plante, de quoi Nous fîmes sortir une verdure, d'où Nous produisîmes des grains, superposés les uns sur les autres; et du palmier, de sa spathe, des régimes de dattes qui se tendent. Et aussi les jardins de raisins, l'olive et la grenade, semblables ou différents les uns des autres. Regardez leurs fruits au moment de leur production et de leur mûrissement. Voilà bien là des signes pour ceux qui ont la foi. (Sourate al-An'am: 99)
Le plafond protecteur: l'ozone
L'air que nous respirons, c'est-à-dire l'atmosphère basse, est dans l'ensemble composé de gaz oxygène. Par gaz oxygène, nous voulons dire O2. Cela veut dire que les molécules d'oxygène de l'atmosphère basse sont constituées de deux atomes. Cependant, la molécule d'oxygène peut quelque fois être constituée de trois atomes (O3). Dans ce cas, la molécule ne s'appelle plus oxygène mais "ozone", car ces deux gaz sont plutôt différents l'un de l'autre.
Un fait doit être ici mentionné: puisque l'oxygène est formé quand deux atomes d'oxygène s'assemblent, pourquoi est-ce qu'un gaz différent appelé ozone se forme quand trois atomes d'oxygène se réunissent? Au final, n'est-ce pas l'atome d'oxygène qui se combine, par deux ou par trois dans une molécule? Pourquoi donc deux gaz différents émergent-ils? Avant de répondre à ces questions, il est préférable de voir ce qui différencie ces deux gaz.

4) O3 5) Chlorine 6) O2
Comment le chlore détruit-il l'ozone?
Le chlore réagit avec l'ozone en produisant une molécule d'oxygène et un ion hypochlorite (OCl-) (1). L'ion réagit avec un atome d'oxygène (2) afin de produire du chlore libre (3), lequel peut réagir avec et détruire une autre molécule d'ozone.32
L'oxygène (O2) se trouve dans l'atmosphère basse et donne la vie à tous les êtres vivants à travers la respiration. L'ozone (O3) est un poison à l'odeur très désagréable. Il se trouve dans la strate la plus haute de l'atmosphère. Si nous devions respirer de l'ozone à la place de l'oxygène, aucun d'entre nous ne survivrait.
L'ozone se trouve dans l'atmosphère supérieure, car il sert une fonction hautement vitale pour la vie. Il forme une couche à environ 20 km au-dessus de l'atmosphère en entourant la Terre comme une ceinture. Il absorbe les rayons ultraviolets émis par le Soleil, les empêchant d'atteindre la Terre avec leur intensité maximale. Puisque les rayons ultraviolets possèdent une très grande énergie, leur contact direct avec la Terre brûlerait toute chose, en empêchant la vie de se former. Pour cette raison, la couche d'ozone sert de barrière protectrice dans l'atmosphère.
Afin que la vie existe sur la Terre, tous les êtres vivants doivent être capables de respirer et d'être protégés des rayons de soleil nuisibles. Celui qui a formé ce système est Dieu, qui commande chaque atome, chaque molécule. Sans la permission de Dieu, aucune puissance ne pourrait assembler ces atomes selon diverses proportions en molécules d'oxygène et d'ozone.
Les molécules que nous goûtons et sentons
Les sens du goût et de l'odorat sont des perceptions qui rendent le monde de l'homme plus beau. Les plaisirs qui découlent de ces sens ont été un sujet d'intérêt depuis les temps anciens et on n'a découvert que récemment qu'ils sont causés par des interactions moléculaires.
Le "goût" et "l'odorat" ne sont que des perceptions qui sont créées par différentes molécules dans nos organes des sens. Par exemple, les odeurs de la nourriture, des boissons ou des fruits et des fleurs que nous voyons autour de nous consistent toutes en molécules volatiles. Comment cela se produit-il?

LA PIPÉRINE
La pipérine est le composant actif du poivre blanc et noir (les baies des vignes tropicales Piper Nigrum). Le poivre noir est obtenu en fermentant le fruit non mûr puis en le séchant. Le poivre blanc est obtenu en enlevant les peaux et la pulpe des baies mûres et en sachant les graines.33
Les molécules volatiles comme les arômes de la vanille et de la rose atteignent les récepteurs situés sur les poils vibrants dans la région nasale appelée l'épithélium et interagissent avec ces récepteurs. Cette interaction est perçue comme une odeur par notre cerveau. Jusqu'ici, sept types différents de récepteurs ont été identifiés dans notre cavité nasale, qui est bordée par une membrane odorante de 2-3 cm2. Chacun de ces récepteurs correspond à une odeur primaire. De la même manière, il existe quatre types différents de récepteurs chimiques dans l'extrémité de notre langue. Ils correspondent aux goûts salés, sucrés, acides et amers. Notre cerveau perçoit les molécules arrivant sur les récepteurs de nos organes réceptifs en tant que signaux chimiques.

Para-HYDROXYPHÉNOL -2-BUTANONE et IONONE
Le mélange de ces deux molécules produit un arôme très agréable. Le butanone est la molécule qui est principalement responsable de l'odeur des framboises mûres. La nouvelle odeur toute fraîche d'un fruit fraîchement cueilli est partiellement due à l'ionone, qui est également responsable des odeurs du foin séché au soleil et des violettes. L'ionone est le composant parfumé de l'huile des violettes.34

FURYLMETHANETHIOL
Cette molécule est l'une de celles responsables de l'arôme du café. L'action stimulante du café est due à la caféine. La couleur des grains de café moulus qu'on voit sur la gauche est largement due à la réaction de brunissement qui se produit lorsque des substances organiques contenant de l'azote sont chauffées. Les molécules responsables de l'odeur et de la stimulation sont piégées de manière temporaire à l'intérieur des grains.35
Réfléchissons une minute. Nous pourrions vivre dans un monde sans saveur ou sans odeur. Puisque nous n'aurions aucune idée des concepts de goût et de bonne odeur, nous ne souhaiterions même pas posséder ces perceptions. Cependant, ce n'est pas le cas. Depuis un sol brun à l'odeur unique apparaissent des centaines de types de fruits, de légumes et de fleurs aromatiques et délicieux avec des centaines de couleurs, de formes et de senteurs différentes. Pourquoi ces atomes, qui d'un côté s'assemblent d'une manière extraordinaire pour former la matière, se combinent, d'un autre côté, pour produire le goût et les odeurs? Bien que nous les considérions comme acquis et que nous ne nous rappelions pas souvent quelle grande faveur ils représentent, ils contribuent agréablement à notre monde en tant que produits d'un art magnifique.
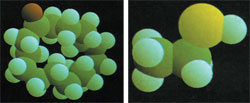
La photo ci-dessus appartient à une molécule de mauvaise odeur et celle de gauche appartient à une molécule aromatique. Ce qui distingue une mauvaise odeur d'une bonne odeur (marqué en marron sur la photo de gauche), ce sont ces petites différences dans un microcosme qui nous est invisible.
Nous pourrions nous nourrir d'un seul type d'aliments. Avez-vous déjà imaginé comment votre vie serait ordinaire et fade si vous deviez manger un seul type de nourriture toute votre vie et boire que de l'eau? Par conséquent, le goût et l'odeur, comme tous les autres bienfaits, sont des bénédictions de Dieu, Celui qui possède une grâce et une bonté infinie, et qui a tout donné à l'homme sans rien en retour. L'absence de ces deux sens rendrait la vie humaine plutôt terne. En retour de tous ces bienfaits qui lui sont accordés, ce qui incombe à l'homme est d'essayer de devenir une personne dont Dieu sera satisfait. En compensation de cette attitude, notre Seigneur nous promet une vie éternelle, qui sera comblée avec des bienfaits illimités, de loin supérieurs à ceux qui nous sont offerts sur la terre comme exemples des délices à venir dans l'au-delà. Cependant, la récompense pour une vie passée en n'étant que peu reconnaissant, de manière insouciante et négligente envers Dieu, sera certainement un juste châtiment:
Et lorsque votre Seigneur proclama: "Si vous êtes reconnaissants, très certainement J'augmenterai Mes bienfaits pour vous. Mais si vous êtes ingrats, Mon châtiment sera terrible." (Sourate Ibrahim: 7)
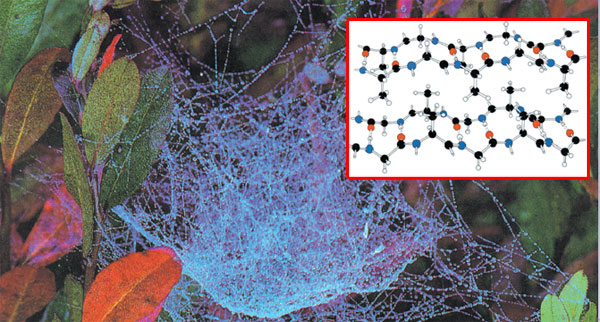
b-KÉRATINE
La soie, nom commun de la b-Kératine, est le liquide solidifié sécrété par un certain nombre d'insectes et d'araignées, le plus précieux étant celui du ver à soie, la chenille du papillon de soie. C'est un polypeptide fabriqué à partir de glycine, d'alanine et à partir de plus petites quantités d'autres acides aminés. Les molécules de b-Kératine ne forment pas d'hélice; au lieu de cela elles sont reliées par les extrémités les unes aux autres afin de former des feuilles enchaînées d'acides aminés reliés entre eux, avec une molécule de glycine apparaissant uniquement sur un côté des feuilles. Ensuite, ces feuilles s'empilent les unes sur les autres. Cette structure plane se ressent quand vous touchez la surface lisse de la soie.36
Comment percevons-nous la matière?
Ce que nous avons dit jusqu'ici a révélé que ce que nous appelons matière n'est pas une entité ayant une couleur, une odeur et une forme spécifique, comme on le croyait. Ce que nous imaginons être de la matière, notre propre corps, notre chambre, notre maison, et en général le monde et l'univers entier, n'est en réalité rien d'autre que de l'énergie. Qu'est-ce qui rend donc toutes les choses autour de nous visibles et palpables?
La raison pour laquelle nous percevons les choses autour de nous comme de la matière est la collision des électrons dans les orbitales des atomes avec des photons, et l'attraction et la répulsion des atomes entre eux.
Et lorsque votre Seigneur proclama: "Si vous êtes reconnaissants, très certainement J'augmenterai Mes bienfaits pour vous. Mais si vous êtes ingrats, Mon châtiment sera terrible." (Sourate Ibrahim: 7)
Vous ne touchez même pas le livre que vous pensez tenir dans votre main en ce moment… En vérité, les atomes de votre main repoussent les atomes du livre et vous ressentez le toucher en fonction de l'intensité de cette répulsion. Comme on l'a mentionné quand nous parlions de la structure des atomes, ils peuvent se rapprocher les uns des autres autant que le diamètre d'un atome. De plus, les seuls atomes qui peuvent se rapprocher autant sont ceux qui réagissent entre eux. Par conséquent, quand bien même les atomes d'une substance ne pourraient en aucune manière se toucher les uns les autres, il serait totalement impossible pour nous de toucher la substance que nous tenons, serrons ou levons dans notre main. En fait, si l'on pouvait se rapprocher autant que possible de l'objet qui est dans notre main, nous serions impliqués dans une réaction chimique avec cet objet. Dans ce cas, il serait impossible pour un être humain ou un autre être vivant de survivre même pendant une seconde. L'être vivant réagirait immédiatement avec la substance sur laquelle il marchait, était assis ou allongé, et serait transformé en autre chose.
L'image finale qui émerge de cette situation est extrêmement remarquable: nous vivons dans un monde qui est composé de 99,95 % de vide rempli d'atomes qui ne sont pratiquement constitués que d'énergie.37 Nous ne touchons en réalité jamais les choses dont nous disons que nous les "touchons et les tenons". À quel point percevons-nous donc la matière que nous voyons, entendons ou sentons? Est-ce que ces substances sont réellement comme nous les voyons ou les entendons? Absolument pas. Nous avons abordé ce sujet quand nous avons parlé des électrons et des molécules. Rappelez-vous, il est littéralement impossible pour nous de voir la matière en l'existence de laquelle nous croyons, car le phénomène que nous appelons "voir" comprend des images formées dans notre cerveau par des photons venant du Soleil, ou d'une autre source de lumière, qui frappent la matière, laquelle absorbe une certaine portion de la lumière et nous renvoie le reste qui vient frapper nos yeux. C'est-à-dire que la matière que nous voyons consiste seulement en informations transportées par des photons qui sont réfléchis vers notre œil. Ainsi, quelle fraction des données liées à la matière nous est-elle communiquée par cette information? Nous n'avons aucune preuve que les formes originales de la matière existant au dehors nous sont totalement renvoyées.
NOTES
24. Martin Sherwood & Christine Sulton, The Physical World, Oxford University Press, 1988, p. 81 ![]()
25. Martin Sherwood & Christine Sulton, The Physical World, Oxford University Press, 1988, p. 82 ![]()
26. Martin Sherwood & Christine Sulton, The Physical World, Oxford University Press, 1988, p. 79 ![]()
27. L. Vlasov, D. Trifonov, 107 Stories About Chemistry, 1977, p. 117 ![]()
28. L. Vlasov, D. Trifonov, 107 Stories About Chemistry, 1977, p. 118 ![]()
29. David Burnie, Life, Eyewitness Science, London: Dorling Kindersley, 1996, p. 8 ![]()
30. Nevil V. Sidgwick, The Chemical Elements and Their Compounds, vol. 1, Oxford: Oxford University Press, 1950, p. 490 ![]()
31. Martin Sherwood & Christine Sulton, The Physical World, Oxford University Press, 1988, p. 30 ![]()
32. Structure of Matter, The Time Inc. Book Company, 1992, p. 76 ![]()
33. P.W. Atkins, Molecules, Scientific American Library, p. 115 ![]()
34. P.W. Atkins, Molecules, Scientific American Library, p. 128 ![]()
35. P.W. Atkins, Molecules, Scientific American Library, p. 130 ![]()
36. P.W. Atkins, Molecules, Scientific American Library, p. 93 ![]()
37. Taşkın Tuna, Uzayın Ötesi (Au-delà de l'espace), Boğaziçi Yayınları, 1995, p. 166 ![]()
